CSIS (Clinical Study Information System)
臨床研究資訊系統 (Clinical Study Information System, CSIS)
系統簡介
臨床研究資訊系統(Clinical Study Information System, CSIS)為美國國家衛生研究院所開發的臨床管理資訊系統(CIMS)中的一項子系統,具備強大的電子表單(eCRF)設計功能,適用各式個案報告表(Case Report Form, CRF)與國際標準問卷,亦可設計CDISC-Compliant eCRF (aCRF),並佐以邏輯化資料檢核功能,簡化過往紙本收案的繁瑣程式與保存負擔,使試驗團隊能更輕鬆省力管理所收集的臨床資料,進而能達到完整性、正確性與可靠性等品質要求。
CSIS系統自2007年由楊永正副教授導入台灣,至今CIMS團隊已協助多項國內由主持人發起(IIT)的臨床試驗(或研究),與各類臨床試驗聯盟執行的疾病登錄計畫(Registry Study);團隊秉持著不斷創新與進步的宗旨,定期導入國際臨床資料標準新知,希望提升國內的臨床試驗品質,同時透過多年來累積的實務經驗來改良CSIS系統,打造了符合我國臨床研究實務操作的臨床資訊登錄平臺,使用者遍佈各大醫學中心,迄今已為國內多數臨床試驗聯盟建立大型疾病登錄資料庫。

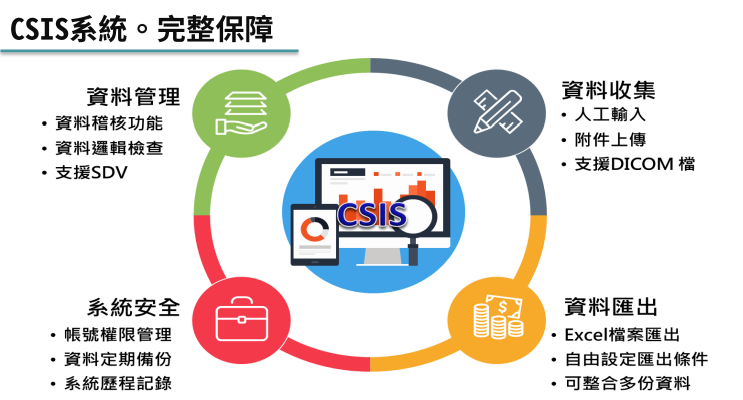
系統特色
- 可搭配API導入外部資料
- 支援批次匯入臨床資料
- 支援各大網路瀏覽器,有網路即可隨時登錄、管理資料
- 具受試者個資保護功能
- 可設計註釋CRF(aCRF)
- 靈活的帳號權限設定,適用各種實際工作配置
- 可搭配檢體管理追蹤管理系統(STAMS),實現資料檢體合一追蹤
- 臨床試驗/臨床研究/人體生物資料庫均可使用
- 團隊經驗豐富,提供完善的IT及管理流程諮詢服務,讓研究者降低試驗成本
- 操作介面友善,可使用行動裝置填寫問卷
服務項目
- 設計電子個案報告表
- 系統教育訓練
- 協助資料管理
- 其他客製化服務
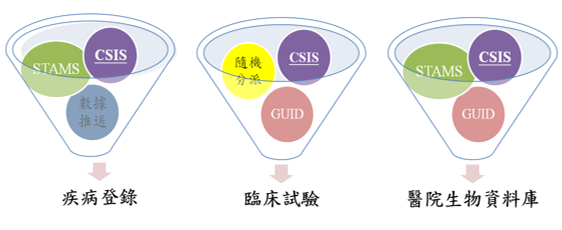
服務對象
臨床研究
- 臨床試驗(Clinical Trial)
- 單疾病
- 單或多中心
- 收集治療組
- 收集研究群體(Cohort)
- 疾病登錄(Registry)
人體生物資料庫
- 虛擬人體生物資料庫
- 單疾病
- 多中心
- 醫院人體生物資料庫
- 多疾病
- 單中心

教育訓練
每月固定於陽明大學舉辦,視需求決定課程。課程時間每月公布於網站,可進行報名。
